Onco – Pédiatrie
Fiche réalisée selon le plan MGS
Item ECNi 294
NB : seuls les aspects généraux des cancers pédiatriques sont traités ici, certaines localisations ou étiologies font l’objet de fiches dédiées (cf. Item 294)
Epidémiologie
– Incidence (Fr, 0-18 ans) = 2500 / an, < 1 % de l’ensemble des cancers, 2e cause de mortalité entre 1 et 15 ans
– 1500 cas / an avant 15 ans, dont la moitié surviennent avant 5 ans. Les cancers les plus fréquents varient selon l’âge *
– Sex-ratio masculin = 1,2 1A, prédominance chez les garçons des lymphomes, médulloblastomes, tumeurs d’Ewing et sarcomes des tissus mous, et chez les filles des tumeurs germinales et épithéliales 0.
– Essentiellement sporadiques, < 10 % surviennent dans le cadre de syndromes génétiques
– 60 % de tumeurs solides, 40 % d’hémopathies malignes (leucémies, lymphomes)
* On retrouve schématiquement
– Avant 5 ans : leucémies aiguës, tumeurs embryonnaires (neuroblastome, néphroblastome, rhabdomyosarcome), certaines tumeurs cérébrales (médulloblastome, gliome de bas grade)
– Après 10 ans : tumeurs cérébrales (gliomes, médulloblastomes), sarcomes osseux (ostéosarcome, sarcome d’Ewing) et des tissus mous (rhabdomyosarcome, autres), lymphomes (Hodgkiniens ou non), tumeurs
Répartition des cancers de l’enfant
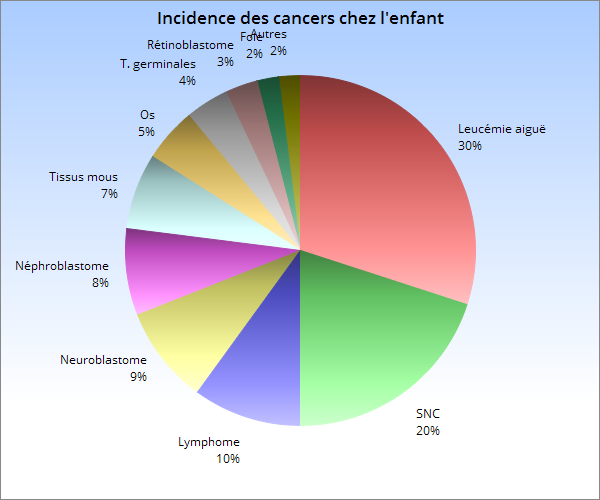 Chez l’adolescent, la répartition est différente 1B
Chez l’adolescent, la répartition est différente 1B
– Lymphomes (23%)
– Tumeurs germinales (13%)
– Leucémies (12%)
– Tumeurs cérébrales (11%)
– Tumeurs osseuses (10%)
– Sarcome des tissus mous (8%)
A ) Clinique
Les signes d’appels sont nombreux, ils peuvent être de découverte fortuite par les parents ou le médecin, ou devant la persistance sous traitement bien conduit d’un symptôme d’allure initialement bénigne.
> Facteurs de risque
Facteurs génétiques
– Formes héréditaires de rétinoblastome (mutation RB1 0) : risque accru de 2nd cancer
– Syndrome de Li-Fraumeni (anomalie p53 0) : tumeurs des tissus mous et des os, lymphomes, tumeurs du SNC, corticosurrénalomes
– Syndrome de Beckwith-Wiedemann : néphroblastomes, hépatoblastomes
– Trisomie 21 : leucémies
– Neurofibromatoses de type 1 et 2 : tumeurs du SNC
– Autres (rares)
Facteurs environnementaux
– Irradiations à forte dose
– EBV : lymphome de Burkitt, carcinome indifférencié du nasopharynx, maladie de Hodgkin
– VIH : lymphomes, léiomyosarcome
– VHB : hépatocarcinome
> Les signes généraux sont beaucoup plus rares que chez l’adulte : AEG ou mauvaise prise staturo-pondérale, infections anormalement répétées.
> Signes « directs » de la tumeur
Masse abdominale
– Intrapéritonéale : lymphome de Burkitt, hépatoblastome
– Rétropéritonéale : néphroblastome, neuroblastome
– Abdomino-pelvienne : tumeur germinale maligne, neuroblastome, sarcome
Tuméfaction des membres ou des parois
– Tissus mous : rhabdomyosarcome ++
– Os : ostéosarcome, tumeur d’Ewing
ADP ‘froides’ (dures, adhérentes, souvent sans inflammation ni douleur)
– Leucémie
– Lymphome
Autres
– Leucocorie (reflet blanc pupillaire) : rétinoblastome
– Augmentation du volume scrotal : rhabdomyosarcome, tumeur germinale maligne, lymphome
– Hématurie : néphroblastome
– Masse péri- ou intra-orificielle ± saignement : rhabdomyosarcome, tumeur germinale maligne vaginale
> Signes « indirects » de la tumeur
Signes neuro
– HTIC, signes neurologiques déficitaires : tumeur cérébrale
– Compression médullaire : tumeur osseuse rachidienne, neuroblastome, hémopathies malignes, tumeurs médullaires
Signes respiratoires
– Dyspnée par compression médiastinale : lymphome (non-Hodgkinien ++), rarement tumeur germinale maligne, sarcome, neuroblastome
– Obstruction respiratoire haute, troubles de déglutition : lymphome ou rhabdomyosarcome ORL
Signes ophtalmo
– Protrusion oculaire : tumeur orbitaire primitive (rhabdomyosarcome) ou méta orbitaire (neuroblastome, hémopathie maligne)
– Strabisme : rétinoblastome
Autres
– Douleurs osseuses localisées : tumeur osseuse (ostéosarcome, tumeur d’Ewing)
– Douleurs osseuses diffuses ± boiterie : atteinte médullaire (leucémie, neuroblastome, sarcome métastatique)
– Troubles sphinctériens : tumeurs abdominopelviennes (sarcome, neuroblastome, tumeur germinale maligne), tumeurs intracanalaires
– Prurit : maladie de Hodgkin
B ) Paraclinique
Les examens paracliniques sont bien entendu orientés selon les hypothèses étiologiques, la confirmation histologique est le plus souvent nécessaire.
> Particularités biologiques
3 principaux marqueurs tumoraux
– α-foeto-protéine (αFP) : tumeurs germinales malignes à composante vitelline, hépatoblastome
– β-hCG : tumeurs germinales malignes à composante choriocarcinome
– Métabolites des catécholamines et dopamine urinaire : neuroblastome
Autres marqueurs moins spécifiques souvent recherchés
– Hypercalcémie : atteinte ostéomédullaire étendue, tumeurs rhabdoïdes
– Elévation des LDH (marqueur d’agressivité) : lymphome non-Hodgkinien, neuroblastome, tumeur d’Ewing
> Particularités d’imagerie
Radiographie standard (souvent très contributif) : Rx de thorax, de segment osseux, ASP
Echographie ± doppler +++ : précise le caractère intra- ou rétropéritonéal d’une lésion abdominale, l’origine d’une tumeur abdo-pelvienne, explore les lésions cervicales, des membres et des parois
Autres (selon les 1ères explorations)
– TDM
– IRM : tumeur du SNC, tumeurs osseuses ou des tissus mous
– Scintigraphie : au technétium (tumeur osseuse primitive ou métastatique), au MIBG = méta-iodobenzylguanine (neuroblastome)
– TEP ± TDM : validée pour les lymphomes Hodgkiniens ou non, de plus en plus utilisée pour d’autres types tumoraux (sarcomes ++)
> Particularités cyto-histologiques
Explorations cytologiques : myélogramme (leucémie), ponction ganglionnaire ou tumorale (certains lymphomes non-Hodgkiniens)
Explorations histologiques : abords biopsiques percutanés ou chirurgicaux a minima
Le pronostic est globalement meilleur que les cancers de l’adulte, avec un taux de guérison de 80 % en occident.
> Situations d’urgence
Dyspnée asphyxiante : lymphome non-Hodgkinien médiastinal, tumeur ORL
Pancytopénie, CIVD : hémopathie maligne
HTIC avec signes neurovégétatifs, convulsions : tumeur cérébrale
Fracture osseuse pathologique : tumeur osseuse
Hémorragie intra-abdominale : néphroblastome
Hypercalcémie : origine paranéoplasique ou lyse osseuse
> Séquelles à long terme liées à la maladie et/ou au traitement
Toxicité d’organe : cardiaque (anthracyclines), rénale (platines, ifosfamide), pulmonaire (irradiation, busulfan, bléomycine, nitroso-urées)
Atteinte fonctionnelle : neurocognitives (HTIC, irradiation, chimio), auditives (platines, irradiation, tumeur ORL ou du SNC), visuelles (tumeurs du SNC, rétinoblastome), endocriniennes (tumeur ou irradiation hypothalamo-hypophysaire, irradiation thyroïdienne, atteinte gonadique par chimio ou irraadiation)
Toxicité sur l’ADN sain : retentissement sur la fertilité (cryopréservation de sperme ou de tissu gonadique avant certains traitements), sur-risque de cancers secondaires
Atteintes esthétiques (traitements locaux)
PEC dans un centre de référence en cancérologie pédiatrique.
!!! Les urgences symptomatiques doivent être traitées en priorité !!!
> Traitement curatif
Les cancers de l’enfant sont caractérisés par un grande chimiosensibilité : la PEC générale comporte, selon le plan de traitement (Programme Personnalisé de Soins)
– Chimiothérapie néo-adjuvante le plus souvent
– Chirurgie d’exérèse si indiquée et réalisable
– Traitements adjuvants : chimio (le plus souvent), radiothérapie (de moins en moins)
Effets secondaires de certaines chimiothérapies
– Hémato : neutropénie fébrile, anémie, thrombopénie
– Digestifs et nutritionnels : nausée / vomissement, anorexie, mucite, troubles du transit
– Alopécie
– Allergie
– Atteinte des fonctions rénale ou hépatique
– Cystite hématurique avec certains agents alkylants
– Toxicité neurologique périphérique, rarement centrale
> Soins palliatifs
20 % des enfants atteints de cancer décèdent après un traitement palliatif d’un cancer d’emblée réfractaire ou en rechute. La phase palliative reste longtemps imprévisible dans sa durée et sa symptomatologie.
Traitements symptomatiques au 1er plan
– Douleur : antalgiques de palier adapté, co-antalgiques ± radiothérapie de certaines zones spécifiques
– Hypoxie : oxygénothérapie, éventuellement évacuation d’un épanchement pleural, péricardique ou péritonéal compressif
– PEC psychologique de l’enfant et de sa famille ± psychotropes
– Chirurgie : dérivation urinaire interne ou externe, dérivation digestive, décompression médullaire
– Traitements sédatifs en situation de fin de vie
Traitements spécifiques oncologiques : peuvent contribuer au ralentissement de l’évolution de la maladie, et au contrôle des symptômes douloureux et d’inconfort





Une réponse à “Cancers de l’enfant : vue d‘ensemble”
Si je ne me trompe pas, c‘est l‘hCG global (et pas seulement la sous-unité béta) qui est mesuré dans ce cadre